CURIOSIDADES
EDUCAÇÃO: Tabela periódica faz 150 anos; conheça algumas curiosidades
PUBLICADO
7 anos atrásem
Em 1869, o químico russo Dmitri Mendeleev apresentou a 1ª versão da tabela, organizando os elementos então conhecidos numa forma bem próxima da atual.
Há 150 anos, quando pouco mais de 60 elementos químicos eram conhecidos, o químico russo Dmitri Mendeleev, professor da Universidade de São Petersburgo, apresentou ao mundo a primeira versão de um dos maiores ícones da ciência moderna: a tabela periódica.
Àquela altura, a alquimia, uma espécie de ancestral mística da química, já havia ficado pra trás, e o conhecimento científico se acumulava rapidamente. Poucos, porém, se dedicavam a sistematizar o que já havia sido descoberto.
No fim do século 18, Lavoisier e outros cientistas já separavam os elementos em grupos como metais e gases, mas ainda se sabia pouco sobre suas propriedades químicas —como os elementos interagem uns com os outros e também a presença de características semelhantes em diferentes elementos.
O que Mendeleev fez foi criar um sistema que, além de catalogar os elementos, permitiu a previsão de propriedades como densidade, reatividade e estabilidade por causa da organização deles, como explica Henrique Toma, professor titular de química da USP, entusiasta de tudo que envolve a tabela periódica e colecionador de elementos químicos, exibidos em um grande mostruário em forma de tabela periódica no Instituto de Química da universidade.
Personagens dos livros de “Game of Thrones” em forma de tabela periódica.
Pela sequência proposta por Mendeleev, os elementos que estão um ao lado do outro na linha horizontal têm propriedades químicas que se repetem de tempos em tempos, a tal periodicidade. E os elementos com características semelhantes ficam na mesma coluna, ou grupo.
Um dos grupos mais famosos é o dos metais alcalinos, o primeiro da tabela e lembrado até por quem saiu da escola faz tempo graças à frase Hoje Li Na Kama Robinson Crusoé em Francês —um jeito de decorar a ordem de lítio, sódio, potássio, rubídio, césio e frâncio. O hidrogênio não é um metal, mas fica logo ali acima e entrou na brincadeira.

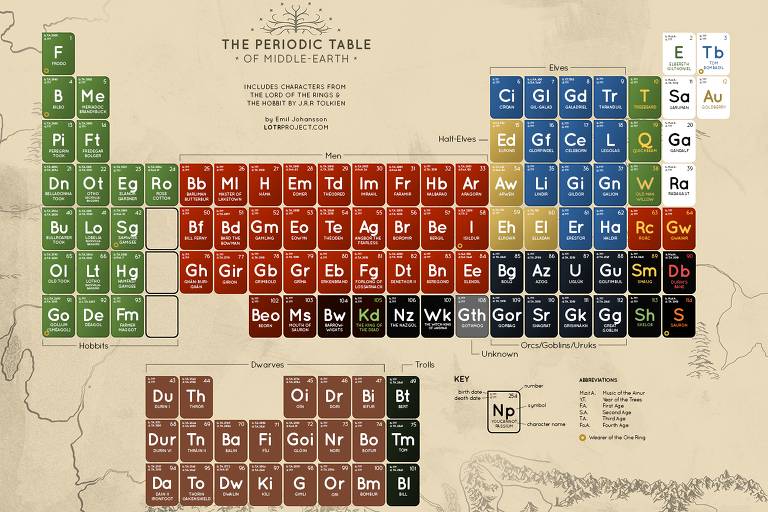
Personagens do livro “O Senhor dos Anéis” em forma de tabela periódica.
Todos os metais alcalinos compartilham características como a formação de sais com os elementos da família dos halogênios e a alta reatividade de suas formas metálicas puras na água, que podem causar intensas explosões graças à formação de gás hidrogênio (H2).

Tabela periódica de molhos em episódio dos Simpsons.
Em 1869, fazia poucas décadas que o sódio (Na), o potássio (K) e o magnésio (Mg) haviam sido isolados em suas formas metálicas pelo britânico Humphry Davy. Para isolar o sódio, ele esquentou e derreteu soda cáustica (NaOH) com o auxílio de uma corrente elétrica, técnica conhecida como eletrólise.
Essa é só uma das maneiras de separar elementos químicos que muitas vezes só aparecem na natureza conjugados a outros átomos, como óxidos, sais e minerais —basicamente, terra e pedras.
Outro jeito de identificar elementos é promover reações com ácidos, capazes de corroer materiais e liberar gases, queimá-los e analisar a cor da chama, além de esquentar, fundir e separar elementos —técnicas aprendidas e refinadas desde a Idade do Bronze, milênios antes de 1869.
O primeiro elemento descoberto por um indivíduo provavelmente foi o fósforo (P), em 1669. O alquimista alemão Hennig Brand processou centenas de litros de urina em uma sucessão de etapas até obter poucos gramas do elemento. Duzentos anos depois, em 1869, já se sabia que carbono, silício e estanho apresentavam algumas propriedades químicas semelhantes, especialmente a forma como se ligam a outros elementos, como o oxigênio e o hidrogênio.
Linha do tempo
1789 – Antoine Lavoisier (1743-1794)
No século 18 nasceu a ciência que hoje conhecemos como química. Lavoisier catalogou os elementos por tipos como metais, não metais e gases
1869 – Dmitri Mendeleev (1834-1907)
Foi quem apresentou uma forma mais inteligente de reunir os elementos, organizando os cerca de 60 conhecidos de acordo com sua massa e suas propriedades químicas — como reagem com outros elementos
1904 – William Ramsay (1852-1916)
Ao longo das décadas seguintes, Mendeleev continuou aperfeiçoando sua tabela. Uma das mais importantes adições foi o grupo dos chamados gases nobres, como o hélio e o argônio, isolados pelo químico escocês William Ramsey e colaboradores
1925 – Henry Moseley (1887-1915)
Antes de morrer na 1ª Guerra Mundial, aos 27 anos, Moseley estabeleceu com uma técnica chamada espectroscopia de raio X que a sequência de elementos químicos na tabela e suas propriedades tinham a ver com a carga de seus núcleos, e não exatamente com a massa
1955 – Glenn Seaborg (1912-1999)
Ao longo do século 20, diversos elementos químicos foram descobertos (inclusive pela síntese de elementos não presentes na natureza). As descobertas do americano Glenn Seaborg e seu grupo permitiram que a tabela ganhasse seu formato atual, com as últimas linhas dos lantanídios e actinídios
Publicações em revistas especializadas e alguns congressos acadêmicos tentavam dar ordem ao conhecimento que se multiplicava, mas só em 1892 houve um encontro, realizado em Genebra, na Suíça, para lidar com a questão dos nomes dos elementos. A Iupac (União Internacional de Química Pura e Aplicada), responsável por reconhecer as descobertas e aprovar os nomes, só nasceria em 1919.
Visionário, Mendeleev pensava que elementos químicos, unidades formadora de compostos como sais, óxidos e ácidos, poderiam ser categorizados apenas pela massa atômica. Mesmo com conhecimento escasso, previu que alguns deles deveriam ser descobertos com determinados valores de massa —um deles era acertadamente o germânio.
A ideia era boa, mas não estava correta. O que define a maior parte das propriedades químicas de um elemento é a quantidade de prótons no núcleo de um átomo, conhecimento que só veio décadas depois. Mesmo assim, a tabela de Mendeleev, que foi sendo aperfeiçoada ao longo do tempo, já era muito próxima da que temos hoje, com os grupos químicos (colunas) apresentados praticamente da forma como conhecemos.
A partir do urânio (92), os elementos não foram descobertos por reações químicas ou decompondo substâncias por eletrólise, mas, sim, criados em laboratório a partir da colisão entre átomos e entre átomos e partículas subatômicas —as chamadas reações nucleares.
Quem tem especial interesse nessa área são os físicos nucleares, mas são os químicos que estão sempre a postos para batizar e reconhecer elementos.
A desavença entre as sociedades de química (Iupac) e física (Iupap) teve auge no fim de 2015 e no início de 2016, quando a primeira anunciou sozinha o reconhecimento dos elementos 113, 115, 117 e 118, antes mesmo do aval do comitê formado por cientistas também da Iupap.
É também a partir do urânio que os elementos criados começam a ser batizados com nomes inspirados em pessoas ou lugares: férmio (do físico italiano Enrico Fermi), mendelévio (do criador da tabela, Mendeleev), nobélio (do sueco Alfred Nobel, inventor da dinamite e idealizador do prêmio Nobel), rutherfórdio (do físico Ernest Rutherford), seabórgio (o primeiro a homenagear uma pessoa viva, o químico americano Glenn Seaborg), tennessínio (em homenagem ao estado do Tennessee) entre muitos outros.
Todos os elementos a partir do urânio são radioativos, e alguns, especialmente os mais pesados, são particularmente instáveis, decompondo-se em frações de segundo, o que torna muito difícil a identificação e a caracterização físico-química deles.
Mesmo assim, nas últimas décadas, houve grande empenho em completar a sétima linha da tabela, em especial de grupos alemães, russos, americanos e japoneses. O feito se deu com a descoberta do oganessônio (elemento 118), em 2002, e seu reconhecimento formal em 2016.
Agora os físicos nucleares miram nos elementos de número 119 em diante, mas obtê-los não será fácil. A meta é encontrar e caracterizar a chamada ilha de estabilidade desses elementos superpesados, ou seja, a combinação ideal de prótons e nêutrons em cada núcleo a fim de fazer elementos mais duráveis.
150 anos da tabela periódica
Conheça cada um de seus 118 elementos.




Foi usado em lanternas, em bebidas supostamente fortificantes e até em pasta de dente. É um metal bastante abundante, tanto que os cientistas tentaram fazer reatores nucleares para usar tório em vez de urânio, sem sucesso.

Um das formas como aparece na natureza é o fósforo branco: tóxico e capaz de pegar fogo espontaneamente, ele é usado em bombas. O fósforo vermelho, menos perigoso, aparece nas caixas de fósforos de segurança, de uso doméstico.

A pouca disponibilidade do ouro no mundo explica seu preço elevado tudo o que já foi minerado caberia em três piscinas olímpicas. Por não oxidar, ele mantém seu brilho eternamente, o que o torna muito útil em contatos elétricos.
Com esse conhecimento, além de um aprendizado importante sobre física quântica, pode ser descoberto algum meio de se obter energia nuclear de forma mais eficiente.
A partir do conhecimento atual, contudo, é difícil até mesmo definir o que seria estabilidade nesses casos —se esses elementos durariam dias, horas ou meros segundos. De todo modo, cientistas já caminham para o número 119 e além.
Apesar de hoje já se saber quase tudo com relação aos elementos químicos, na área de nanomateriais (estruturas com dimensões da ordem de nanômetros, ou milionésimos de milímetro) ainda há muito a ser explorado, diz o químico da USP Henrique Toma.
Esses materiais apresentam propriedades eletrônicas, mecânicas e ópticas (forma como interagem com a luz) bem diferentes dos elementos em suas apresentações usuais. Toma aposta que essa é a próxima fronteira da pesquisa ligada aos elementos químicos.
Os grupos de cada cor
Hidrogênio
Diferentemente dos outros componentes da coluna, ele tem a forma de gás. Compõe a maior parte do Universo visível, e é a partir da energia que resta da transformação dele em hélio (He) no Sol que recebemos luz e calor na Terra
Metais alcalinos
Tirando o hidrogênio, os elementos da primeira coluna —lítio, sódio, potássio, rubídio, césio e frâncio— são os metais alcalinos que, em contato com a água, formam gás hidrogênio, altamente inflamável. São leves, brilhantes e moles
Metais alcalinos terrosos
Nesta família estão berílio, magnésio, cálcio, estrôncio, bário e rádio. Todos ocorrem na natureza. Esses metais tendem a ser prateados e também são relativamente moles e reagem com a água liberando hidrogênio (com exceção do berílio)
Elementos (ou metais) de transição
O bloco central da tabela tem os famosos ferro, ouro, cobre, platina e titânio. Eles tendem a ser duros e sólidos (a exceção é o mercúrio, líquido à temperatura ambiente); muitos deles fazem parte da indústria siderúrgica
Terras raras
As duas últimas linhas são dos elementos conhecidos como terras raras. Os actinídios, que abrangem urânio e plutônio, são radioativos. Entre os lantanídios está o neodímio, elemento a partir do qual são feitos poderosos imãs
Metais ordinários
Ocupando um “triângulo” na tabela periódica e com elementos como alumínio, estanho e chumbo, esses metais são moles ou quebradiços e são facilmente fundidos.
Metaloides
Elementos dessa “diagonal” estão numa área cinzenta entre os metais e os não metais. Têm aparência metálica, mas não conduzem bem a eletricidade. São quebradiços e hoje são usados em lentes e em semicondutores.
Não metais
Carbono, nitrogênio, oxigênio, fósforo, enxofre e selênio—, assim como os das duas colunas seguintes —funcionam como isolantes térmicos e elétricos. Tendem a ser reativos e, desses seis, apenas o oxigênio é gasoso à temperatura ambiente
Halogênios
Flúor, cloro, bromo, iodo e astato também são não metais, mas têm características especialmente reativas e formam sais com outros elementos (como o sódio, que forma o NaCl, o sal de cozinha).
Gases nobres
Hélio, neônio, argônio, criptônio, xenônio, radônio —são pouco reativos, o que permite que sejam usados para criar ambientes inertes, que protegem outras substâncias.
Relacionado
CURIOSIDADES
Explorando o Mundo Digital com Betandyou: Muito Além do Básico
PUBLICADO
2 anos atrásem
17 de setembro de 2024Em um mundo digital cada vez mais diversificado, encontrar uma plataforma que atenda a diferentes necessidades pode ser um desafio. O Betandyou surge como uma solução completa para quem quer ir além do básico e descobrir novas formas de interação online. Em Portugal, essa plataforma se destaca não apenas pela sua ampla oferta de serviços, mas também pela experiência personalizada que oferece a seus usuários.
Variedade de Opções Para Todos os Gostos
Um dos grandes diferenciais do Betandyou é a sua variedade de opções. A plataforma não se limita apenas às tradicionais apostas esportivas, embora ofereça um leque abrangente para os amantes do esporte. No entanto, o Betandyou vai além, permitindo que os usuários explorem outros tipos de conteúdo e entretenimento.
Os eSports, por exemplo, são uma área em crescimento na plataforma. Para quem acompanha esse tipo de competição digital, o Betandyou oferece diversas oportunidades de engajamento. Assim, os usuários podem acompanhar partidas de seus jogos favoritos, como League of Legends ou Dota 2, e até mesmo interagir com essas competições de maneiras inovadoras.
Outro destaque são os eventos virtuais. Com a tecnologia cada vez mais presente no cotidiano, eventos online tornaram-se uma forma popular de interação. No Betandyou, os usuários podem explorar uma série de eventos que vão desde shows ao vivo até exposições digitais. Esse tipo de variedade é ideal para quem busca algo diferente e quer experimentar novas formas de entretenimento.
Tecnologia e Segurança em Primeiro Lugar
A segurança online é uma prioridade para os usuários modernos, e o Betandyou entende essa necessidade. A plataforma utiliza sistemas avançados de criptografia para garantir que todos os dados pessoais e financeiros dos usuários estejam protegidos. Isso é especialmente importante em Portugal, onde a regulamentação para plataformas online tem se tornado cada vez mais rigorosa.
Além da segurança, a tecnologia do Betandyou também permite que a navegação seja rápida e sem complicações. Com um design responsivo, a plataforma se adapta a diferentes dispositivos, garantindo que a experiência seja igualmente agradável em um computador ou em um smartphone. Isso facilita o acesso a qualquer momento e de qualquer lugar, permitindo que o usuário aproveite o que a plataforma tem de melhor.
Promoções e Vantagens Exclusivas
Para os usuários em Portugal, o Betandyou oferece uma série de promoções exclusivas que tornam a experiência ainda mais agradável. Desde bônus em apostas até vantagens em eventos específicos, a plataforma sabe como atrair e manter seu público engajado. Uma das promoções mais populares são os bônus para novos usuários, que permitem começar a explorar a plataforma com vantagens adicionais.
Além disso, o Betandyou conta com um programa de fidelidade que recompensa os usuários mais frequentes. Com esse programa, é possível acumular pontos que podem ser trocados por prêmios, entradas em eventos especiais e até mesmo crédito adicional na plataforma. Esse tipo de incentivo mantém os usuários engajados e oferece uma experiência personalizada e gratificante.
Suporte e Atendimento ao Cliente
Outro aspecto que merece destaque no Betandyou é o suporte ao cliente. Disponível em português, a equipe de atendimento está sempre pronta para ajudar em qualquer dúvida ou problema que os usuários possam enfrentar. Esse suporte é fundamental para garantir que a experiência do usuário seja a melhor possível, desde o primeiro acesso até o uso diário da plataforma.
Conclusão
Com uma oferta variada de serviços, segurança de ponta e promoções exclusivas para o público português, o Betandyou se consolida como uma das principais plataformas de entretenimento online em Portugal. Mais do que apenas um site de apostas, o Betandyou oferece uma experiência completa e personalizada, atendendo a diferentes gostos e necessidades. Seja para quem busca diversão, engajamento em esportes ou explorar novos horizontes digitais, o Betandyou é uma escolha confiável e diversificada.
Relacionado
BRASIL
Domine o JetX Bet: Estratégias e Dicas para Lucrar Mais
PUBLICADO
2 anos atrásem
20 de dezembro de 2023Introdução ao JetX Bet – Inovação em Apostas Online
Bem-vindos ao universo revolucionário do jetx aposta Bet, um jogo de apostas que mistura adrenalina e estratégia, proporcionado pela SmartSoft Gaming. Este artigo é um guia completo para quem deseja não só se divertir, mas também aumentar suas chances de ganhos significativos.
O Que é o JetX Bet?
JetX Bet é um jogo de apostas dinâmico onde os jogadores apostam no progresso de um foguete. O objetivo é retirar a aposta antes do foguete explodir, o que pode ocorrer a qualquer momento. Este jogo desafia tanto a sorte quanto a estratégia do jogador.
Características Principais do Jogo
- Provedor: SmartSoft Gaming
- Retorno ao Jogador (RTP): 97%
- Faixa de Apostas: R$0,50 a R$300
- Ganho Máximo: Multiplicador de até x100
- Compatibilidade: Disponível em dispositivos móveis e PC
Estratégias Avançadas para Sucesso no JetX
Apostas Estratégicas
- Equilíbrio entre Risco e Recompensa: A chave para maximizar os ganhos é alternar entre multiplicadores altos e baixos, equilibrando o risco.
- Método Martingale: Essa estratégia clássica de dobrar a aposta após uma perda pode ser eficaz, mas requer cautela e um bom gerenciamento de bankroll.
Mecânicas do Jogo
- Retirada Automática vs. Manual: Decidir entre a retirada automática e manual é crucial para otimizar os ganhos e minimizar as perdas.
Gerenciamento de Bankroll
- Apostas Sensatas: Alinhe suas apostas com o seu bankroll total para garantir uma experiência de jogo sustentável.
Dicas dos Profissionais: Aprimorando a Experiência no JetX
- Paciência: Aguarde o momento ideal para retirar a aposta.
- Observação: Aprenda com os padrões de apostas de outros jogadores para obter insights valiosos.
- Jogo Responsável: Mantenha-se dentro dos seus limites para uma experiência positiva de jogo.
JetX no Celular – Jogue em Qualquer Lugar
O aplicativo móvel do JetX traz toda a emoção do jogo para a palma da sua mão. Com jogabilidade fluida e interface amigável, jogue JetX onde quer que esteja.
Aprofundando nas Táticas de Apostas no JetX
A maestria no JetX não se resume apenas em saber quando apostar, mas também em como apostar. Uma tática eficaz envolve a diversificação das apostas. Ao invés de concentrar todo o seu bankroll em uma única rodada, distribua suas apostas em múltiplas rodadas com diferentes estratégias de multiplicadores. Isso não só aumenta suas chances de ganhos em várias rodadas, mas também reduz o risco de perdas significativas. Além disso, uma abordagem mista de apostas manuais e automáticas pode ser benéfica. Enquanto as apostas manuais permitem um controle direto e a emoção de decidir no momento, as apostas automáticas garantem que você não perca o momento ideal de saída, especialmente em situações onde a distração é possível.
Outro aspecto a considerar é o acompanhamento constante das tendências e padrões do jogo. O JetX, embora baseado na aleatoriedade, pode apresentar certos padrões que, se identificados, podem ser explorados para maximizar os ganhos. Estar atento às estatísticas do jogo, como a frequência das explosões do foguete em diferentes multiplicadores, pode oferecer insights valiosos para ajustar suas estratégias. Além disso, a participação em fóruns e comunidades online dedicadas ao JetX pode fornecer dicas e estratégias compartilhadas por outros jogadores experientes.
Garantindo o Jogo Justo no JetX
- Tecnologia Provably Fair: O JetX utiliza esta tecnologia para garantir a justiça e a transparência em cada rodada.
- Geração de Números Aleatórios: O resultado de cada jogo é determinado por um sistema sofisticado de RNG, assegurando a aleatoriedade e imparcialidade.
Conclusão Sobre o JetX
O JetX oferece uma mistura empolgante de estratégia, sorte e entretenimento. Embora o jogo tenha riscos inerentes, estratégias inteligentes de apostas e gerenciamento de bankroll podem melhorar significativamente suas chances de ganhar. Aceite o desafio, aproveite a emoção e que a sorte esteja a seu favor na sua jornada com o JetX!
Relacionado
BRASIL
A Aplicação da Máquina de Gravação a Laser UV em Tampas de Garrafas Garante a Segurança do Produto e a Imagem da Marca
PUBLICADO
2 anos atrásem
20 de dezembro de 2023Com o desenvolvimento contínuo do mercado de consumo, as tampas de garrafas, por serem uma barreira importante para proteger o conteúdo de garrafas, desempenham um papel importante na qualidade e na segurança do produto. O método tradicional de gravação de tampas de garrafas tem seus problemas, por exemplo, a impressão por transferência térmica pode se soltar facilmente e a impressão não fica clara. As máquinas de gravação a laser UV surgiram para solucionar facilmente esse problema. Como um método de gravação eficiente e de alta precisão, a tecnologia de gravação a laser UV é amplamente usada em vários setores.
Mas a gravação na tampa da garrafa feita por uma máquina a laser UV não é apenas o nome do produto ou sua data de fabricação, mas também um reflexo da qualidade e da autenticidade do produto. As vantagens da aplicação das máquinas de gravação a laser UV em tampas de garrafas se refletem principalmente nos seguintes aspectos:
- A máquina de gravação a laser UV tem como características alta velocidade e alta eficiência.
A aplicação de máquinas de gravação a laser UV pode completar a gravação de uma grande quantidade de tampas de garrafas em pouco tempo, melhorando imensamente a eficiência da produção. Ao mesmo tempo, a impressora a laser UV tem uma alta velocidade de gravação, padrão de gravação nítido e dificilmente borra ou se solta, solucionando efetivamente problemas que ocorrem com tecnologias de impressão tradicionais.
- A máquina de gravação a laser UV possui capacidades de gravação de alta precisão.
A máquina de gravação a laser UV usa um método de gravação sem contato, que possibilita gravar letras, padrões, QR codes, etc., na superfície de tampas de garrafas com alta precisão, tornando a tampa de garrafa mais personalizada e bonita, e possibilitando até mesmo o controle de produto e de mercado por meio de QR codes. Além disso, o equipamento de gravação a laser UV também pode gravar fontes pequenas e padrões complexos para atender às necessidades de diferentes clientes.
- A máquina de gravação a laser UV também tem como características a proteção do meio ambiente e a economia energética.
Em comparação com os métodos de impressão tradicionais, as máquinas de gravação a laser UV usam uma tecnologia de gravação a laser sem poluição e sem exaustão, que não produz substâncias nocivas e resíduos, atendendo aos requisitos de proteção ambiental e também reduzindo os custos de produção da empresa.
![]()
- A máquina de gravação a laser UV pode atender a necessidades de customização personalizadas.
A tampa de uma garrafa é um aspecto importante de um produto. Além de transmitir informações básicas, o design do rótulo também pode refletir a imagem e a personalidade da marca. Máquinas de gravação a laser de alta velocidade proporcionam uma seleção mais rica de estilos e padrões de gravação para atender ao posicionamento da marca e às necessidades de mercado de diferentes empresas.
- A máquina de gravação a laser UV tem boa adaptabilidade e flexibilidade.
Tampas de garrafas de diferentes formas e materiais podem ser gravadas pela máquina de gravação a laser UV. Não importa qual seja o material delas, plástico ou cerâmica, a máquina se adequa às necessidades de produção. Além disso, através do sistema de controle do software, a alternância automática de gravação de diferentes padrões, textos e QR codes pode ser realizada facilmente, melhorando a flexibilidade e a diversidade da produção.
Resumindo, as vantagens da aplicação de máquinas de gravação a laser sem contato na produção de tampas de garrafas se refletem principalmente na velocidade, eficiência, baixos custos e adaptabilidade. Ao usar uma tecnologia de gravação a laser UV, a segurança do produto pode ser garantida, uma boa imagem de marca pode ser estabelecida e a competitividade comercial pode ser otimizada. Além disso, com o constante desenvolvimento e inovação da tecnologia, nós acreditamos que a tecnologia de gravação a laser UV terá um espaço de aplicação mais amplo.
![]()
![]()
A CYCJET é marca registrada da Yuchang Industrial Company Limited. Como fabricante, a CYCJET tem mais de 19 anos de experiência em diferentes tipos de P&D para soluções de impressão inkjet portátil, soluções de impressão a laser, soluções de marcação portátil e soluções de Impressão em Alta Definição em Shanghai, China.
Pessoa para Contato: David Guo
Telefone: +86-21-59970419 ext 8008
MOB:+86-139 1763 1707
E-mail: sales@cycjet.com
Web: https://cycjet.com/
Vídeo de Referência: https://youtu.be/rgiBHuT9iSs
Linkedin: https://www.linkedin.com/feed/update/urn:li:activity:7135898632473497601
Ins: https://www.instagram.com/reel/C0QwMftsvSX/?igshid=MTc4MmM1YmI2Ng==
Alibaba:
Made-in-China:
Você precisa fazer login para comentar.